法令遵守体制の強化に関する協会の取組みについて
はじめに
昨年12月に当協会の会員会社(当時)で発生した事案では、調査を行った第三者委員会からコンプライアンス・ガバナンスの欠如が指摘されています。
コンプライアンス・ガバナンスの確保は、適正な企業活動を行う上で基本であり、かつ、重要なことであると当協会は強く認識しています。会員会社は、各社でコンプライアンス・ガバナンスの確保に対して十分な認識を有することが必要であることは言うまでもありませんが、会員会社各社がその重要性を認識し、しっかりとした取組みを進めるために、当協会としても会員会社の状況を確認した上で、コンプライアンス・ガバナンスに関する研修の充実、会員会社からの相談体制の強化などを進め、外部に対して目に見えるかたちで公表していくべきであると考えています。
相談体制の強化に関しては、コンプライアンス・ガバナンスに関連すると思われる具体的な事例の受け皿として「協会への問合せ対応の充実」を図るとともに、会員会社からのGMPに関する技術的な相談の受け皿として「品質委員会におけるGMP相談窓口の新設」を行いました。
さらに、当協会では「各社の内部通報制度への対応状況の確認とその制度の充実支援」を行ってまいります。
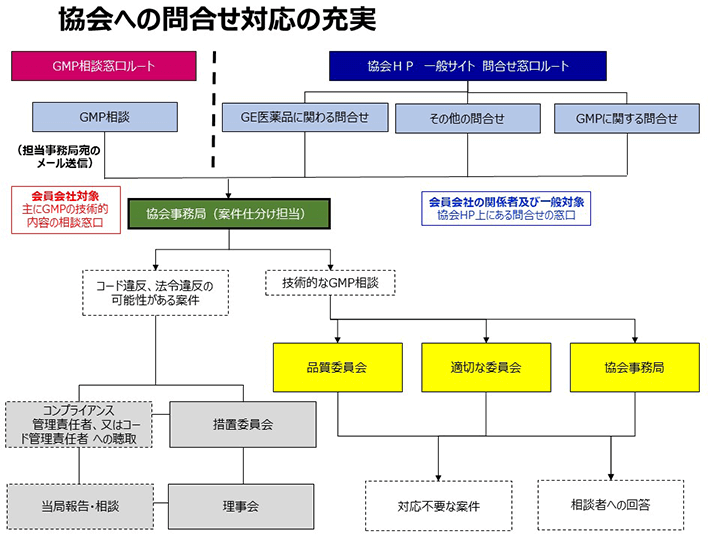
協会への問合せ対応の充実
当協会では、これまで、協会ホームページ(HP)上に協会内外からのお問い合わせを承るサイトを設置し、「ジェネリック医薬品に関するお問い合わせ」や「ご要望」などにお答えしてまいりました。
今回、そのサイトにこれまでいただいているお問い合わせだけではなく、会員会社で発生したような法令遵守に係る問題が隠蔽されることがないよう、会員会社の関係者から法令やコードに違反する可能性がある案件やGMP上の法令違反の可能性のある内容についても受付可能であることを、HP上にわかりやすく示しました。
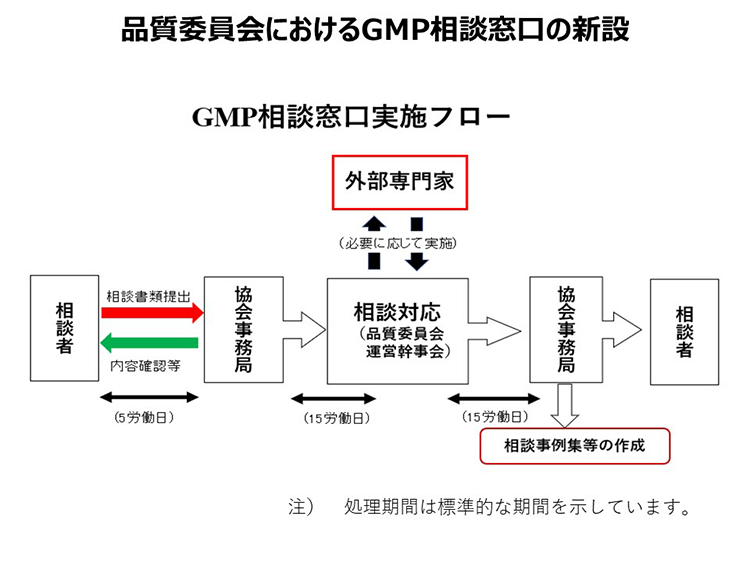
品質委員会におけるGMP相談窓口の新設
会員会社からのGMPに関する技術的な相談の受け皿として、当協会の品質委員会はGMP相談窓口を新設しました。本相談制度は、会員会社を対象としたもので、主にGMPに関する技術的な内容の相談を専用メールアドレスで受け付け、品質委員会運営幹事、又は内容によって外部専門家の意見を求めて回答するものです。本相談窓口は、会員各社の内部通報制度を補完したり、代替するものではありませんが、技術的な内容の中にはコンプライアンスに起因する問題も内在する場合もあります。そのような場合には、品質委員会以外の協会関係者による対応を行う体制を採り対応を行うことにしました。
各社の内部通報制度への対応状況の確認とその制度の充実支援
内部通報制度(公益通報制度)は、社内での不正のリスクを社内でいち早く発見し適切に対処するために、不正行為と思われる案件を発見した従業員等が組織の通常の報告ルートとは異なるルートで報告できるようにする制度です。2020年6月12日に改正公益通報者保護法(以下「改正法」)が公布され、従業員301人以上の企業には内部通報制度の整備が義務づけられました。従業員300人以下の企業は努力義務となっています。改正法は、2022年6月11日までに施行されます。この制度が適切に運用・活用されることにより、社内の不正行為等を未然に防ぐことが可能となります。
当協会では、会員会社の内部通報制度への現時点での対応状況を調査しました(「内部通報制度対応アンケート調査結果について」をご参照ください。)。当協会は、改正法に沿ってそれぞれの会員会社が義務規定又は努力義務規定の適用にかかわらず、適切に内部通報制度を運用できるよう支援してまいります。特に、内部通報制度を運用する上で最も重要な「通報者保護」や「秘密保持の徹底」等について、各会員会社の理解を深めるための研究会等も実施してまいります。
各社におけるコンプライアンス自己点検の実施
生命関連製品を取り扱う製薬企業は、他の業種より一層高い倫理観をもって事業活動を行うことが求められており、当協会でも「GE薬協企業行動憲章」「GE薬協コンプライアンス・プログラム・ガイドライン2021」「ジェネリック製薬企業における企業行動基準のモデル」等のGE薬協自主行動基準を定めてきました。
当協会では、GE薬協コンプライアンス・プログラム・ガイドライン2021を参考に、会員各社がコンプライアンス活動を自己点検するための「コンプライアンス自己点検チェックリスト(モデル案)」を作成しました。
今回、協会発第62号通知(令和4年9月21日付)により、信頼回復に向けた取組みの最重要課題であるコンプライアンス・ガバナンス・ リスクマネジメントの強化に関して、自己点検の実施を検討するよう依頼しております。
お問い合わせ
いずれのお問い合わせにつきましてもこちらのフォームからお願いいたします。