委員会活動
日本ジェネリック製薬協会(GE薬協)の委員会活動は16の常設委員会および2つの非常設委員会にて構成されており、会員各社から参画した委員によって、日々、ジェネリック医薬品の様々な課題や関係団体との折衝など業界の発展に貢献しています。
組織図
※マウスを委員会・部会に合わせると活動内容が表示されます。
※委員会・部会をタッチすると活動内容にリンクします。
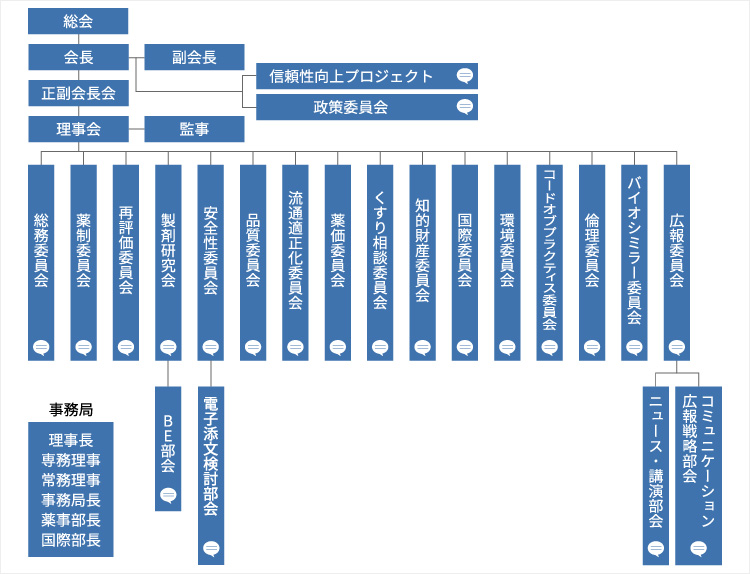
※2025年6月現在
総務委員会
当協会の運営に関わる諸問題及び将来課題の対応に関して、協会内外と各種調整を行います。
薬制委員会
医薬品の承認・業許可に関する事項、及びその他薬機法に関する事項に関して、問題点の抽出・整理を行い、会員企業の活動の効率化・承認審査の迅速化に寄与しております。また、日薬連等の他業界団体との連携・協力を踏まえ、当局への提言等を行っています。
再評価委員会
医薬品の再評価全般(有効性、安全性、品質)に関する事項 について検討・対応を行っています。
製剤研究会
医薬品開発過程での技術・研究課題や関連学術論文などに関する議論を行い、国内外の関連行政の動向や規制について情報共有することで、より優れた医薬品の開発に貢献することを目的とします。
BE部会
製剤研究会活動のうち、生物学的同等性試験などの臨床試験関連・生物薬剤学関連分野などについて専門的に取り扱います。
安全性委員会
医薬品の安全性・適正使用に関する、GVP、GPSP、RMP、安全性情報、電子添文等の事項について、日薬連等の他業界団体と連携・協力のもと様々な検討を行っています。また、テーマを定め標準化検討を行い、会員企業の活動の標準化・レベルアップに寄与しています。
電子添文検討部会
ジェネリック医薬品の電子添文における情報提供の充実及び質的向上を図るための諸検討を行っています。
品質委員会
GQP「医薬品等の品質管理の基準」、GMP「医薬品等の製造管理及び品質管理の基準」等に係る関連諸問題について検討し、併せて日本薬局方及びICHに関して関連委員会と連携し、会員企業による信頼性の高いジェネリック医薬品の安定供給に役立てることを目的としています。
教育研修部会
会員会社の教育担当者を対象に、クオリティーカルチャーをはじめ様々な題材にて研修やワークショップを行い、会員各社のクオリティーカルチャーの醸成及び教育に資する活動に努めています。
流通適正化委員会
医療用医薬品の流通改善を推進するため、必要な情報と資料の収集・検討し啓発することを目的としています。
薬価委員会
ジェネリック医薬品の薬価に関し、日薬連や関係団体等と連携・協力し、ジェネリック医薬品業界としての意見表明や提案を行い、適切な薬価制度の実現を目指します。
くすり相談委員会
医療関係者ならびに患者からのくすり相談事例の検討と情報の共有化により対応スキルの向上、医薬品の適正使用の推進、医療用医薬品の販売情報提供活動に関するガイドライン等の遵守ひいてはジェネリック医薬品の信頼性向上に努めています。
知的財産委員会
後発医薬品に関する知的財産権上の諸問題について、各種情報を収集・検討し、後発医薬品の使用促進のための提案、提言、各種調整を行っています。
国際委員会
「アジア健康構想」に関わる活動や、IGBA(国際ジェネリック医薬品・バイオシミラー協会)での活動、海外のジェネリック医薬品団体との交流・連携を通じて、世界のジェネリック医薬品の動向や海外進出についての課題を把握し、対応することを目的としています。
環境委員会
地球温暖化、省資源・廃棄物問題などの環境課題に関する情報の収集・啓発を行い、日薬連と連携した業界の取り組みを推進しています。
COP委員会
協会のコード・オブ・プラクティスを管理運営し、会員会社におけるコード遵守推進活動を支援することを目的としています。
倫理委員会
会員企業の企業倫理・コンプライアンスの推進を通じて、ジェネリック製薬企業の社会的信頼の向上を図ることを目的としています。
バイオシミラー委員会
バイオシミラーの課題に関わる情報を国内外から収集し、検討・議論したうえで会員企業や外部ステークホルダーに対して必要な情報発信することを目的としています。
広報委員会
各委員会や特別委員会の対外広報に関する事項、JGAニュースの発行、広告掲載、 学術大会等イベント参加、ホームページ等の企画管理を行っています。
ニュース・講演部会
JGAニュースの編集、ジェネリック医薬品啓発活動(イベント実施、パンフレット作成等)、学術大会への参加、大学での薬学生向け講義対応などを行っています。
コミュニケーション広報戦略部会
ジェネリック医薬品および当産業への正しい理解の促進を目的としたPR活動の企画・実施(SNS含むデジタル施策ほか)、協会Webサイトの企画管理等。
常設委員会以外の活動
信頼性向上プロジェクト
「後発医薬品のさらなる使用促進のためのロードマップ」の課題に対する取組を継続的に行うなど、ジェネリック医薬品の信頼性の向上に努めています。
政策委員会
ジェネリック医薬品・同産業に対する各方面の理解増進を図ることの重要性に鑑み、同産業の将来構想・同産業に関わる重要事項について協会としての主張・見解をまとめること、そのために必要な情報収集分析等を行います。